Machine Learning vs Séméiologie classique en cancérologie ORL!
Ce mois-ci deux revues radiologiques de référence nous proposent des études visant à mieux diagnostiquer les métastases ganglionnaires dans les carcinomes épidermoïdes ORL. Au-delà de l’intérêt clinique, les approches proposées montrent bien les orientations de la radiologie diagnostique en 2019.
La première étude est parue dans European Radiology (rubrique intelligence artificielle), l’abstract peut être visible ici.
Elle est portée par le Dr Reza Forghani de l’université McGill à Montreal, qui se pose via ses publications en leader pour les études de radiomique en radiologie ORL, particulièrement en se basant sur des données de scanners double énergie. La radiomique consiste à extraire une information biologique de statistiques issus des données d’imagerie via ses marqueurs mathématiques/quantitatifs. Certains algorithme de radiomique analyse l’imagerie de façon conjointe avec d’autres informations médicales comme la biologie ou la clinique.
L’idée dans ce papier est d’appliquer la radiomique à l’analyse de texture tumorale, en extrayant le maximum de biomarqueurs quantitatifs de la tumeur en elle-même (et non des ganglions) sur une seule coupe de scanner injecté. On applique ensuite un algorithme dit de « Machine Learning » pour classifier l’ensemble de ces biomarqueurs de façon à prédire le risque d’un envahissement ganglionnaire qui peut être infra-clinique mais aussi infra-radiologique (sans signe de dissémination tumorale ganglionnaire après analyse du radiologue).
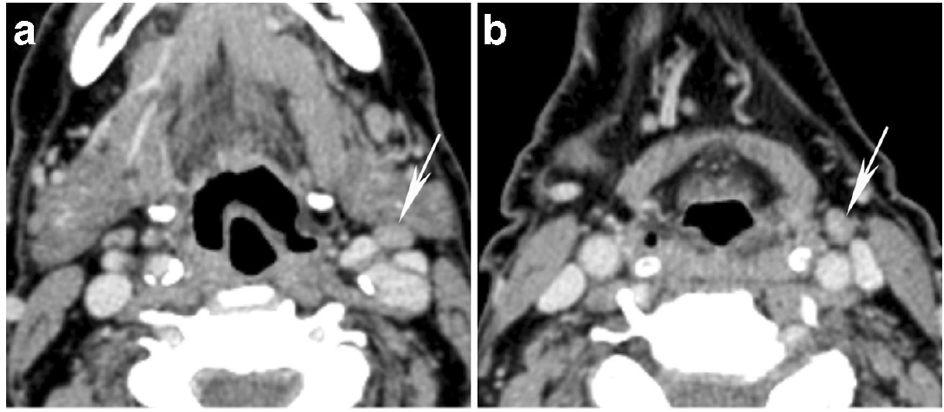
Cet exemple tiré de l’article illustre bien l’intérêt potentiel, les flèches blanches correspondant à des ganglions dont l’anatomo-pathologie a prouvé le caractère micro-métastatique, après que l’algorithme ait prédit un probable envahissement ganglionnaire sur la texture de la tumeur primitive (sans bien sur localiser les ganglions atteints).
On fera plusieurs remarques, d’abord que le succès du Deep Learning en imagerie a remis à la mode des algorithmes de classification plus anciens comme le Random Forest utilisé dans cet article. Il s’agit d’approche différentes, le Deep Learning tient son caractère innovant dans sa capacité à classifier sans nécessiter une sélection préalable des caractéristiques importantes en imagerie (extraction automatique).
Le Random Forest (« forêts aléatoires ») est une méthode statistique de classification qui elle nécessite de donner en entrée les variables d’intérêt pour classifier comme par exemple la densité tumorale ou le volume de la tumeur primitive. On ne peut que conseiller l’excellent article de Radiographics disponible ici (pour les adhérents du Cireol) pour comprendre la différence entre le Deep Learning et les méthodes de Machine Learning classique et se référer à cet article récent de la revue Nature (open source) qui explique pourquoi dans un certain nombre de cas en médecine les méthodes de classifications classiques font mieux que le Deep Learning.
Les auteurs ont donc choisi le Machine Learning classique en choisissant d’extraire à partir d’une seule coupe axiale de la tumeur (dessinée manuellement par un radiologue) des valeurs mathématiques basées sur de multiples images virtuelles monochromatiques (s’agissant de scanner double énergie). Si certaines valeurs sont compréhensibles pour le radiologue telle que la moyenne de densité de la tumeur à chaque faisceau d’énergie (par exemple 40 keV, 65 keV…), le principe de la radiomique est d’associer le maximum de données mathématiques complexes de type Skewness, Kurtosis dont l’interprétation apparaît beaucoup plus malaisée. L’ensemble de ces variables doit caractériser la « texture » de la tumeur.
On ne peut s’empêcher de penser que le modèle statistique utilisé (ils en ont testé des centaines) ne sera pas forcément utilisable sur d’autres scanners doubles énergies réglés différemment, sur d’autres coupes d’intérêt ; et de façon plus générale qu’il serait plus simple de caractériser la tumeur de façon quantitative avec des données plus universelles de type simple scanner injecté et en restant sur la densité Hounsfield intra-tumorale. Les auteurs ont testé l’approche monochromatique à 65 keV, qui s’est révélé moins efficace qu’en utilisant les différents faisceaux d’énergie. Une piste intéressante serait d’utiliser un algorithme non linéaire de réduction de dimension (Manifold Learning) pour analyser l’hétérogénéité de la tumeur à visée diagnostique individuel.
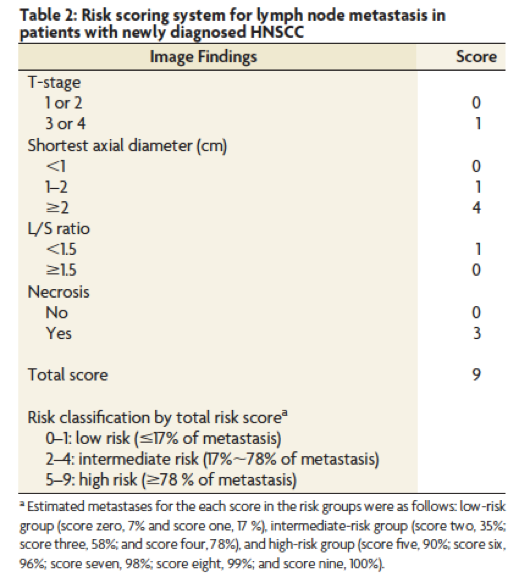
La seconde étude publiée dans l’American Journal of Neuroradiology (abstract ici) par une équipe de Corée du Sud portée par le Dr Chung prends l’exact contre-pied : on revient à l’analyse des ganglions avec une échelle qui reprends tous les critères connus et publiés de malignité pour proposer un « scoring system » en 9 points qui permettra ensuite de proposer une analyse multi-variée et des courbes ROC. Le système de score est disponible ici :
La recherche va tellement vite que l’on a presque l’impression de voir des statistiques « à l’ancienne » sur des biomarqueurs connus : ainsi la présence de nécrose ganglionnaire ou d’un petit diamètre du ganglion supérieur à 2 cm feront vite grimper le score du patient vers un risque élevé de métastases ganglionnaires.
Cette étude a l’avantage majeure de ne nécessiter que des acquisitions scannographiques relativement standard de type injecté. Les inconvénients de ces études « radiologue dépendant » sont connus : difficulté d’identifier les micro-métastases, difficulté de propagation de la méthodologie en l’absence de conférence de consensus.
Au total deux études intéressantes et complémentaires qui sonnent comme un passage de témoin. En attendant que les algorithmes de Machine Learning s’affinent et deviennent plus universels, on gardera un œil vigilant sur les micro et macro-métastases sur nos acquisitions habituelles !
Bien amicalement, Arnaud